Microbiote intestinal et santé mentale – y a-t-il vraiment une liaison ? Et, si la réponse est positive, laquelle et pourquoi ?
La communication entre les intestins et notre cerveau est beaucoup plus intense que ce que l’on croyait auparavant.
Les intestins possèdent un réseau nerveux que les scientifiques qualifient carrément de “deuxième cerveau”. Ces cellules nerveuses émettent des stimuli exerçant une influence sur le fonctionnement intestinal, dont le mouvement du tractus digestif et la libération de certains enzymes.
Le microbiote intestinal possède une fonction protectrice en régulant une population de cellules cérébrales : les astrocytes qui sont un type de cellules gliales. Ces astrocytes permettent de lutter contre l’inflammation cérébrale. Ces cellules sont capables de limiter l’inflammation dans le cerveau en induisant la mort de cellules qui participe à la réponse immunitaire et favorise l’inflammation.
La découverte de ce nouveau mécanisme par lequel l’intestin régule l’inflammation du cerveau est une avancée importante dans la compréhension de la neuro-inflammation.
Microbiote intestinal et santé mentale – Quel est le lien entre le cerveau et l’intestin ?
Notre cerveau n’est pas un organe à part, isolé du reste du corps, coincé dans sa boite crânienne. Il est lié bien sûr à nos organes sensoriels, yeux mais aussi mains – au point, pour cette dernière, qu’elle est surnommée « cerveau externe » depuis le philosophe Emmanuel Kant.
Une étude publiée dans Nature par le gastro-entérologue Emeran A. Mayer explique comment les deux organes, le cerveau et l’intestin, sont reliés. Et il apparaît que cette interaction présente un intérêt pour les deux parties : non seulement pour la régulation des fonctions gastro-intestinales, mais aussi pour notre mental, plus précisément l’humeur et la prise de décision intuitive.
Mais si nos organes sensoriels sont essentiels à notre cerveau pour les informations qu’ils lui envoient sur la réalité qui nous entoure et pour nous permettre d’exprimer nos idées, ils ne sont pas des organes vitaux.
L’intestin est le seul à être dans ce cas. Sa relation avec le cerveau est ainsi d’une nature particulière et bien plus poussée encore que ce qui s’observe avec les autres organes. Regardons dans les détails.
Cellules de l’intestin et neurones du cerveau – les mêmes origines
En premier lieu, rappelons les nombreux liens, physiques, unissent le cerveau et les intestins.
L’intestin est déjà issu de cellules venant d’une structure de l’embryon appelée « crête neurale », qui donnera aussi les neurones et une bonne partie de notre système nerveux périphérique.
Et une fois le corps pleinement développé, il existe un réseau complexe de terminaisons nerveuses tapissant l’ensemble du tube digestif et des zones dans le système nerveux central dédiées au système intestinal. La communication entre cerveau et intestin s’établit à plusieurs niveaux : par des voies nerveuses (notamment le nerf vague), mais aussi par le sang.
Hormones, neurotransmetteurs et … microbiote
Ensuite, il faut souligner une autre particularité de l’intestin, qui s’avère être un organe aux fonctions bien plus complexes qu’on le pense souvent.
Certaines de ses cellules, dites entéro-endocrines, cachées dans ses couches le plus profondes, sont capables de sécréter des hormones. D’autres, comme les cellules entérochromaffines, sont chargées de neurotransmetteurs. Par exemple, des peptides (également présents dans le cerveau) et de la sérotonine – souvent surnommée « hormone du bonheur ».
En fait, l’intestin est l’endroit de notre corps où l’on trouve le plus de sérotonine (plus de 90 %). Le reste se trouve dans le sang et le cerveau (pour seulement 1 %).
Mais ce n’est pas tout. L’intestin, non content de posséder ses propres neurones et neurotransmetteurs plus ou moins connectés au cerveau et avec des neurones et neurotransmetteurs spécifiques, abrite également un grand nombre de micro-organismes. Ces derniers, des bactéries, virus, champignons, etc. plus nombreux que nos propres cellules, constituent ce qu’on appelle le « microbiote ». Ils contribuent à notre bonne digestion, à la lutte contre d’autres agents pathogènes et à de nombreux autres processus.
Et on s’approche un peu à notre thème principal : microbiote intestinal et santé mentale, les connexion méconnues et nettement sous-estimées.
Les intestins et leur microbiote
La tâche importante de l’intestin

La longueur intestinale de chaque être humain est de près de 10 m.
Comme la peau, les cellules intestinales forment un tissu épithélial appelé épithélium intestinal. Cette couche représente, tout comme la peau, une barrière entre notre organisme et le monde extérieur.
Une des tâches de la paroi intestinale est d’extraire les nutriments de notre alimentation ingérée (macronutriments, micronutriments, antioxydants, etc.) afin de permettre le bon fonctionnement de l’ensemble de notre organisme, y compris des cellules, tissus, organes, muscles, et, bien sûr, du cerveau. Cette paroi détient également une fonction importante de barrière contre toute intrusion de microbes comme les bactéries, virus, parasites et champignons.
Pour remplir correctement son rôle, la muqueuse intestinale est constamment renouvelée, au rythme de 70 milliards de cellules par jour !
Un organe constamment en mouvement
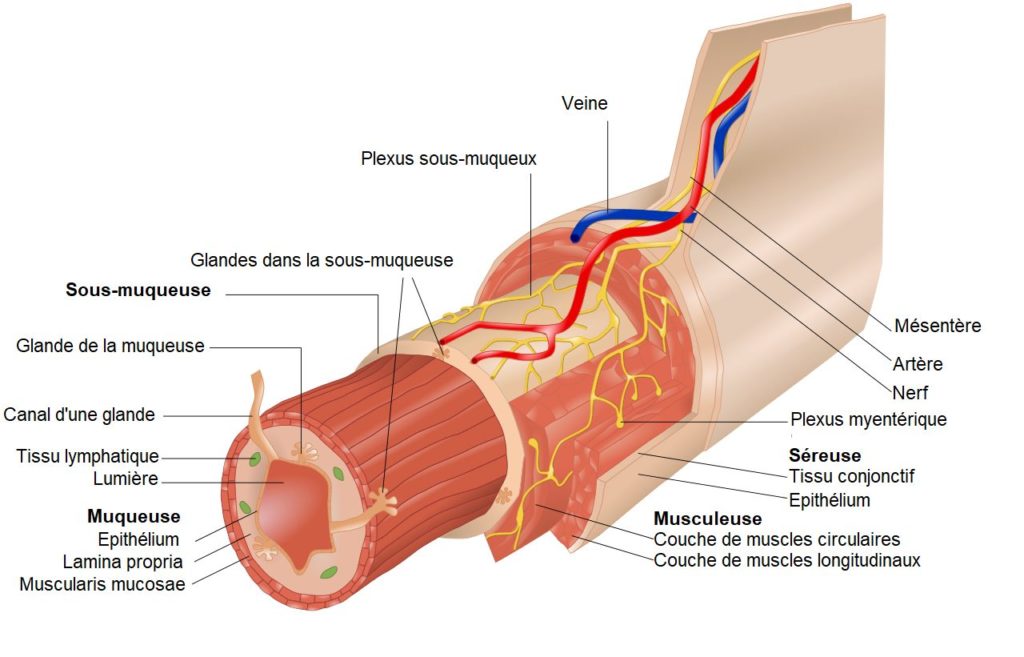
L’intestin est un organe constamment en mouvement.
Au long du trajet dans le tube digestif, des sucs digestifs sont sécrétés pour extraire les nutriments et le liquide des aliments. La paroi intestinale comporte plusieurs types de cellules, et chacune de ces cellules a des fonctions spécifiques. Certaines cellules libèrent les enzymes nécessaires pour décomposer les aliments en unités, qui seront par la suite absorbés dans la circulation sanguine. D’autres produisent du mucus, des hormones ou libèrent des protéines qui neutralisent des agresseurs potentiels.
Pour une bonne organisation du système, une communication entre cerveau et intestins est nécessaire.
De nombreux récepteurs évaluent la situation dans les intestins et relaient ces informations au cerveau qui les analyse et renvoie des signaux afin d’adapter le fonctionnement des intestins.
Notre microbiote intestinal prend de l’importance dans les recherches scientifiques
Qu’est-ce qu’un microbiote ?
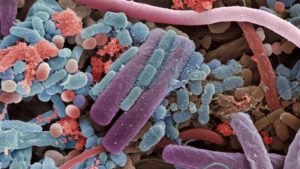
La définition d’un microbiote est l’ensemble des micro-organismes qui peuplent un environnement spécifique.
Plus précisément, il s’agit de bactéries, parasites, virus et champignons qui ne sont pas considérés comme pathogènes ; ils sont complètement inoffensifs. Juste au contraire : ces micro-organismes attribuent à l’équilibre du milieu où ils vivent et à la santé globale de l’être vivant concerné. On appelle ces micro-organismes, inoffensifs et bénéfiques pour la santé, également “commensaux“. On connaît dans notre corps plusieurs milieux anatomiques de microbiotes : notre peau, nez, bouche, pharynx, poumons, vagin, et, bien sûr, nos intestins qui est nettement le plus important.
Le microbiote intestinal – Un micro-cosmos bien peuplé
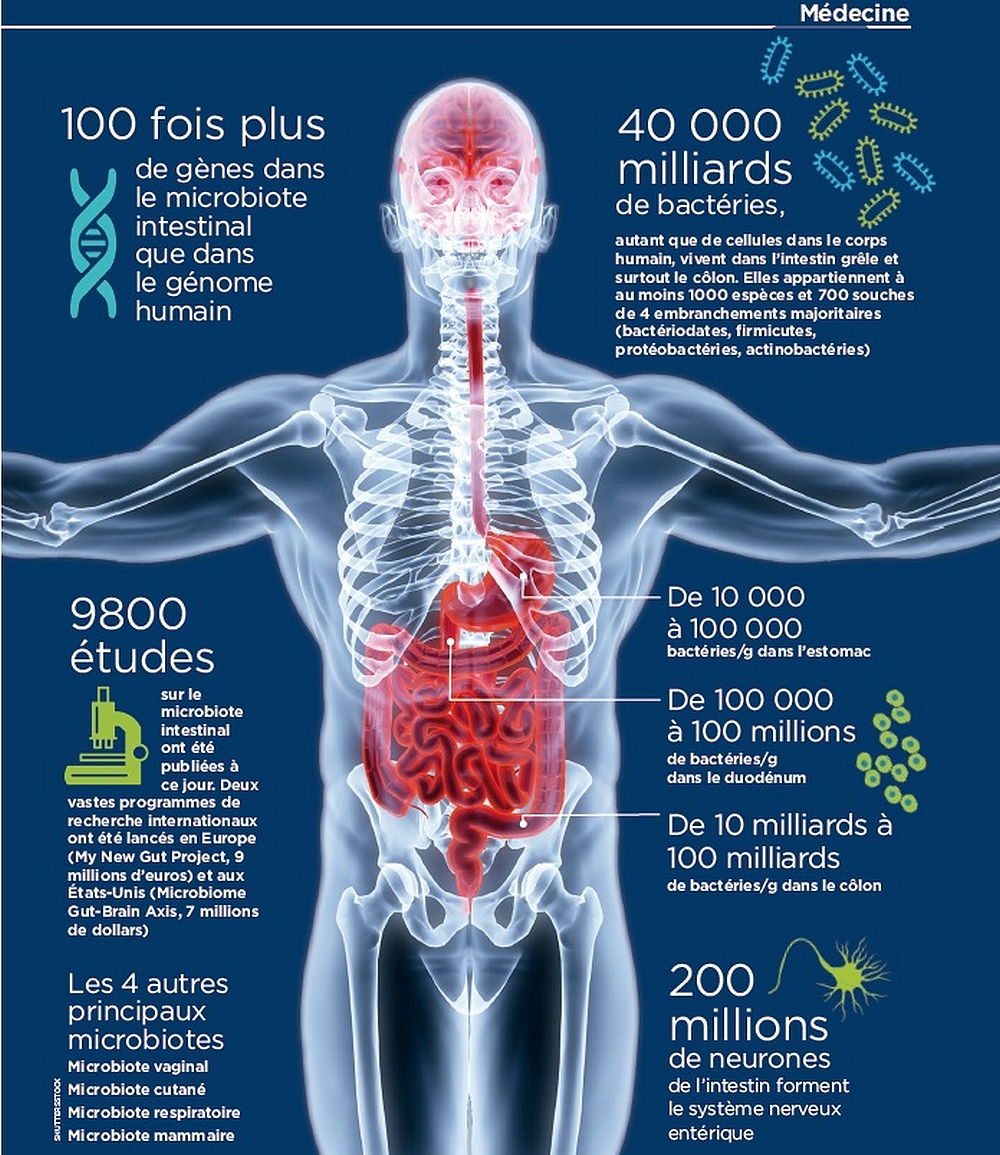
Selon l’Inserm, notre tube digestif abriterait pas moins de 1013 micro-organismes, soit autant que le nombre de cellules qui constituent notre corps.
Cet ensemble de bactéries, virus, parasites et champignons non pathogènes constitue notre microbiote intestinal (ou anciennement flore intestinale).
Ce microbiote intestinal est localisé dans le côlon et l’intestin grêle. L’estomac héberge cent millions de fois moins de micro-organismes commensales, vue la présence de l’acidité gastrique que tout organisme vivant redoute.
Le microbiote intestinal se forme dès la naissance et se développe ensuite selon nos habitudes de vie
Le développement en bonne santé d’un bébé et de l’enfant dépend en grande partie de ses microbiotes.
On estime aujourd’hui que celui de la mère joue un rôle déterminant dans le développement fœtal. A la naissance, le microbiote d’un individu se constitue progressivement, d’abord au contact de la flore vaginale et fécale après un accouchement par voie basse, ou à celui des micro-organismes de l’environnement en cas de naissance par césarienne.
La colonisation bactérienne a lieu graduellement, et se déroule dans un ordre bien précis :
- les premières bactéries intestinales ont besoin d’oxygène pour se multiplier (bactéries aérobies : entérocoques, staphylocoques…). En consommant l’oxygène présent dans l’intestin, elles favorisent ensuite l’implantation de bactéries qui ne prolifèrent justement qu’en absence de ce gaz (bactéries anaérobies : Bacteroides, Clostridium, Bifidobacterium…).
- Pendant les premières années de vie, la composition du microbiote intestinal va ensuite évoluer qualitativement et quantitativement, sous l’influence de la diversification alimentaire, de la génétique, du niveau d’hygiène, des traitements médicaux reçus et de l’environnement. Cette composition reste ensuite assez stable, même si cette stabilité semble variable d’une personne à l’autre.
Certains évènements et nos habitudes de vie ont ensuite un impact sur la composition du microbiote intestinal : les modifications de l’hygiène de vie, notre alimentation, maladies et infections subies, les traitements médicaux (surtout antibiotiques), ou encore les hormones sexuelles peuvent modifier considérablement le microbiote de façon plus ou moins durable.
La recherche scientifique commence à s’y intéresser
Grâce à de nouvelle technologies scientifiques, tel que le séquençage haut débit du matériel génétique, combiné à des analyses métabolomique et lipidomique qui permettent quant à elles d’identifier les substances produites par cet écosystème, les recherches concernant le microbiote intestinal connaissent actuellement un vrai élan.
Par conséquent, le rôle du microbiote intestinal sur notre santé est de mieux en mieux connu et reconnu. On sait désormais qu’il joue un rôle majeur dans les fonctions digestives, d’assimilations nutritives, métaboliques, immunitaires et neurologiques.
La dysbiose, c’est-à-dire l’altération qualitative et/ou fonctionnelle du microbiote intestinal, est devenue une piste sérieuse pour expliquer certaines maladies, notamment parmi celles sous-tendues par des mécanismes auto-immuns ou inflammatoires. Mais une dysbiose peut affecter également la santé digestive, métabolique, immunitaire et neurologique.
On voit donc qu’une grande partie du bon fonctionnement de notre corps et de notre état de santé, autant physique que mental, dépend directement du bon fonctionnement du microbiote. Cette thématique est devenue centrale pour la recherche biologique et médicale.
Communication entre intestin et cerveau : la base pour une relation entre microbiote intestinal et santé mentale
Notre deuxième cerveau

Les scientifiques ont mis en évidence la présence de neurones dans notre intestin, indirectement liés avec le microbiote intestinal. On compterait environ 500 millions de neurones dans nos intestins, constituant ainsi un système nerveux à part entière : le système nerveux entérique. Il s’agit du second système nerveux de l’organisme, d’où le nom de « deuxième cerveau ».
Concrètement, ces neurones présents dans nos intestins s’échangent de manière continue avec nos neurones du cerveau. Pour cela, ils utilisent surtout le nerf vague, mais également les voies sanguines. Ainsi, le système nerveux entérique transmet en permanence un flux d’informations.
Le nerf vague joue un rôle primordial dans l’axe intestin-cerveau. Il relie directement les systèmes nerveux de notre système digestif et de notre cerveau. Les interactions de notre microbiote intestinal avec notre intestin utilisent la voie nerveuse pour envoyer des signaux à notre cerveau et permettre d’informer notre cerveau de notre « santé digestive ».
Ainsi de nombreuses informations, régulant certaines fonctions motrices, sensitives, sensorielles et végétatives (les mécanismes autonomes de notre organisme) sont échangées entre l’intestin et le cerveau.
Une dysbiose du microbiote intestinal altère les informations intestinales
Les scientifiques sont persuadées que la dysbiose du microbiote (déséquilibre du microbiote) pourrait modifier l’information transmise au système nerveux central et au système nerveux entérique, modifiant ainsi le fonctionnement des deux organes. Cela impliquerait une connexion directe entre le microbiote intestinal et la santé mentale.
Les mécanismes impliqués seraient multiples :
- Des composés et métabolites issus du microbiote intestinal ont la capacité de traverser la barrière intestinale. Ces éléments peuvent après influencer, voire moduler le système nerveux entérique. Cela a un impact sur le fonctionnement intestinal et également sur le nerf vague. Par conséquent, il en découlera une modification du fonctionnement du cerveau.
- Ces composés et métabolites peuvent également atteindre le système nerveux central, cette fois par voie sanguine. Une fois parvenus dans le cerveau, ils peuvent s’avérer délétères pour certaines fonctions nerveuses et neuronales.
- Les bactéries peuvent indirectement moduler certaines fonctions endocrines dont le contrôle est notamment assuré par le système nerveux central. Elles ont en effet la capacité à interagir avec les cellules dites entéroendocrines localisées dans la paroi, et qui sont en lien avec le cerveau. Cela a par exemple été décrit pour la voie sérotoninergique.
Ces différents mécanismes confirment la thèse qu’une dérégulation du microbiote intestinale, observée dans des pathologies neurodégénératives (Alzheimer, Parkinson, etc.) et lors de troubles du développement neurologique, peut non seulement contribuer aux troubles digestifs, mais aussi aux symptômes neurologiques.
Microbiote intestinal et inflammation chronique
L’inflammation physiologique : vitale et nécessaire, vs. l’inflammation chronique : le tueur silencieux
L’inflammation est un processus biologique vitale et importante. Elle est étroitement corrélée à l’immunité.
On distingue deux types d’inflammations :
- Inflammation physiologique : ce type d’inflammation est indispensable à l’activation de la réponse immunitaire. Elle permet notamment le contrôle du microbiote, et des réactions inflammatoires importantes, déclenchées en présence d’espèces pathogènes. Ce dernier mécanisme repose notamment sur la présence de composants bactériens inflammatoires. Ces antigènes provoquent une réaction immunitaire qui conduit à la production de médiateurs pro-inflammatoires (cytokines) par les macrophages de l’intestin. Une inflammation locale est déclenchée et la perméabilité de la paroi intestinale augmente. Les LPS peuvent alors traverser cette dernière, passer dans la circulation sanguine, et provoquer un phénomène inflammatoire dans d’autres tissus cibles.
- Inflammation chronique : les origines de l’inflammation chronique sont variées, mais il existe dans tous les cas une persistance du facteur d’agression malgré la défense immunitaire. Cela veut dire que l’élément déclencheur de l’inflammation chronique n’est pas un évènement unique, mais répétitif dans le temps, voire une habitude. Ces facteurs d’agression peuvent être :
-
- toxiques : alcool, tabac, drogues, polluants de l’air extérieur ou intérieur, polluants dans l’alimentation, mauvais composants peu sains de l’alimentation (glucides à index glycémique élevé comme farine blanche, sucre, ou acides gras trans), polluants dans l’eau, prise régulière de médicaments, etc. ;
- infectieux : d’origine bactérienne comme dans la tuberculose, mais qui peut aussi être d’origine virale, fongique, ou parasitaire ;
- auto-immunes : par exemple dans les lupus ou dans la maladie de Crohn ;
- d’origine idiopathique (médicalement parlé incertaine et sans explication d’origine) ;
- le résultat de l’obésité viscérale importante : l’obésité provoque souvent une inflammation chronique du tissu adipeux, contribuant à l’aggravation du syndrome métabolique et du risque d’insulino-résistance.
Le microbiote intestinal a une influence sur l’inflammation cérébrale et donc sur notre santé mentale
En cas de dysbiose du microbiote, les intestins pourraient donc jouer un rôle primordial dans la genèse et le développement de pathologies mentales, psychologiques et neurologiques.
En même temps, de nouveaux travaux de recherche ont réussi à démontrer que le microbiote intestinal peut avoir une fonction protectrice en régulant une population de cellules cérébrales qui permet de lutter contre l’inflammation du cerveau.
Activité anti-inflammatoire des astrocytes, un type de cellules gliales

Dans le cerveau, les neurones sont entourés d’autres types de cellules : les cellules gliales. Ces dernières sont présentes de façon très abondante.
Parmi les cellules gliales, on trouve les astrocytes qui doivent leur nom à leur forme étoilée. Longtemps considérés comme de simples cellules de soutien physique au tissu cérébral, les astrocytes s’avèrent en réalité occuper des fonctions bien plus variées. Ils participent directement à la modulation de l’activité neuronale au sein des synapses. De plus, les astrocytes jouent également un rôle dans le contrôle du flux sanguin cérébral, la régénération du tissu nerveux, ou encore la neuro-inflammation.
Ensuite, il a récemment été montré un rôle anti-inflammatoire des astrocytes.
Le microbiote intestinal régule l’activité anti-inflammatoire des astrocytes
Des scientifiques du Brigham and Women’s Hospital à Harvard Medical School (Boston, USA), ont cherché à mieux caractériser cette fonction protectrice anti-inflammatoire des astrocytes. Ils sont parvenus à mettre en évidence une nouvelle voie anti-inflammatoire régulée par les bactéries résidant dans l’intestin.
En utilisant des techniques perfectionnées d’analyses de gènes, protéines et cellules, ces chercheurs ont réussi à identifier un nouveau sous-ensemble d’astrocytes situé près des méninges (membranes enveloppant le système nerveux central) et exprimant des protéines particulières, LAMP1 et TRAIL.
Ces astrocytes sont capables de limiter l’inflammation dans le cerveau en induisant la mort des lymphocytes T qui participent à la réponse immunitaire et favorisent l’inflammation. Le mécanisme mis en jeu pour contrôler ces astrocytes implique une molécule de signalisation appelée interféron-gamma.
De façon remarquable, les chercheurs ont constaté que c’est le microbiote intestinal qui induit l’expression de cette molécule dans des cellules des méninges. Celles-ci envoient alors un message aux astrocytes exprimant LAMP1 et TRAIL afin d’activer leur pouvoir anti-inflammatoire.
La découverte de ce nouveau mécanisme par lequel l’intestin régule l’inflammation du cerveau est une avancée importante dans la compréhension de la neuro-inflammation. La mise en évidence d’une sous-catégorie d’astrocytes aux fonctions anti-inflammatoires contrôlées par le microbiote intestinal ouvre la voie vers le développement de nouvelles approches thérapeutiques pour lutter contre les pathologies du cerveau, et notamment les maladies neuro-inflammatoires comme la sclérose en plaques.
Des probiotiques pouvant permettre de réguler l’activité anti-inflammatoire de ces astrocytes sont par exemple en cours d’exploration. D’autres données récentes de l’équipe de recherche indiquent que certaines tumeurs cérébrales exploiteraient aussi cette voie pour échapper à la réponse immunitaire du corps. Les applications de ces recherches pourraient donc être utiles à de nombreuses pathologies du cerveau.
Stress, microbiote intestinale et santé mentale

Des pathologies concernant la santé mentale, comme la dépression, les troubles bipolaires ou encore l’anxiété pourraient être concernées par des modifications de la composition du microbiote qui mènent à une dysbiose intestinale.
Bien sûr, le microbiote ne serait cependant qu’un parmi de nombreux autres facteurs qui jouent potentiellement un rôle dans la genèse de ces pathologies. D’autres paramètres à prendre en considération peuvent être des facteurs psychologiques, émotionnels, environnementaux, génétiques, épigénétiques ou encore l’influence d’éléments toxiques.
Les perspectives thérapeutiques sont nombreuses : des études préliminaires ont montré que l’administration de certains probiotiques permettait d’améliorer les symptômes d’anxiété ou de dépression chez des personnes malades.
D’autres ont montré que l’adaptation du régime alimentaire pouvait améliorer le déclin cognitif. Ces pistes restent pour l’heure extrêmement précoces et demandent à être confirmées.
Le stress et son influence sur le microbiote (et vice versa)
Au cours des deux dernières décennies, de nombreuses preuves scientifiques ont été présentées, dans des modèles animaux et chez l’homme, indiquant que lorsqu’un individu subit un stress, l’intestin est en effet altéré et la composition de son microbiote peut même être modifiée.
Des études ont montré qu’un stress subi au début de la vie diminue la concentration de bactéries Lactobacili, laissant ainsi la place à des bactéries pathogènes qui vont venir perturber l’équilibre physiologique entre les différentes populations de micro-organismes présentes.
À l’inverse, la modification expérimentale du microbiote peut également induire des changements de comportement. Ainsi, certains bifidobacteriums sont capables de renforcer le comportement dépressif chez les rats.
Quelle est la liaison entre stress et inflammation chronique ?
Ces dernières années, de nombreux travaux ont indiqué que l’inflammation chronique de faible intensité pouvait également jouer un rôle dans la physiopathologie de la dépression.
Sur la base de ces informations, et connaissant le lien entre dépression et stress, on a cherché à savoir s’il pouvait y avoir un lien entre l’inflammation d’origine intestinale et ce dernier. Et de fait, plusieurs études menées notamment par l’Université Complutense de Madrid ont montré comment il pouvait produire un déséquilibre intestinal.
Cela pourrait entraîner une instabilité de la barrière intestinale, la rendant plus poreuse et perturbant donc le passage des molécules, nutriments et composants divers (parfois d’origine bactérienne) vers la circulation sanguine – et ainsi vers d’autres organes. Ces composants peuvent être toxiques et déclencher une réaction inflammatoire généralisée.
En outre, ces études ont montré que la composition de la flore bactérienne est altérée chez les patients souffrant de dépression par rapport à la flore des individus témoins sains. En général, la diversité bactérienne diminue en cas de dépression. Cependant, nous ne comprenons toujours pas l’association entre le microbiote et l’inflammation dans la dépression.
Dommages importants par oxydation cellulaire chez les personnes dépressives
Nous savons maintenant que les dommages cellulaires oxydatifs (qui sont la conséquence ultime de l’inflammation) sont plus élevés chez les patients présentant un épisode actif de dépression.
Ces personnes présentaient également des niveaux élevés d’un composant de la membrane des bactéries intestinales étroitement lié à la réponse immunitaire : le lipopolysaccharide des bactéries du genre Bilophila et Alistipes. En même temps, on a constaté la diminution des Anaerostipes et la disparition complète des Dialister. Ces altérations n’apparaissent pas chez les patients en rémission de leur maladie.
Il reste à déterminer si les toxines des bactéries présentes dans le microbiote des patients atteints de dépression peuvent circuler dans tout le système nerveux et marquer certaines structures du cerveau.
Pour l’instant, on sait déjà que, dans les modèles animaux, ces bactéries sont bien capables d’atteindre le cerveau et d’activer les récepteurs de la réponse immunitaire dans les neurones et autres cellules cérébrales. Nous savons également que dans le tissu cérébral de patients dépressifs qui se sont suicidés, une hyperactivation de la réponse immunitaire a été identifiée.
Mais nous sommes encore loin de pouvoir affirmer qu’il existe une causalité entre ces phénomènes et la physiopathologie de la dépression. Néanmoins, le défi est là et la tâche de la science biomédicale est de démêler tous ces mécanismes afin d’offrir aux patients de nouvelles et meilleures solutions thérapeutiques.
Autres articles qui pourraient vous intéresser :
Microbiote intestinal – Les recherches scientifiques pour contrôler des maladies chroniques
Sources :
- Quelles sont les particularités du microbiote intestinal d’une personne dépressive ? (theconversation.com) (Creative Commons, CC BY-ND). Juan C. Leza, Catedrático. Dpto. Farmacología y Toxicología. Facultad de Medicina. CIBERSAM., Universidad Complutense de Madrid et Javier R. Caso, Profesor Contratado Doctor. Dpto. Farmacología y Toxicología, Facultad de Medicina. CIBERSAM-ISCIII., Universidad Complutense de Madrid
- Microbiote intestinal (flore intestinale) ⋅ Inserm, La science pour la santé . Dominique Gauguier (unité 1124, Centre universitaire des Saints Pères, Paris), Michel Neunlist (unité Inserm 1235, Institut des maladies de l’appareil digestif, Nantes) , Harry Sokol (unité Inserm 938, Centre de recherche Saint-Antoine, Paris) et Laurence Zitvogel (unité Inserm 1015, Institut Gustave-Roussy, Villejuif)
- Gut feelings: the emerging biology of gut–brain communication | Nature Reviews Neuroscience
- Gut-licensed IFNγ+ NK cells drive LAMP1+TRAIL+ anti-inflammatory astrocytes | Nature
Sources / Crédits images :
- Illustration 3D Tissu du jéjunum : Flickr, by NIH (National Institutes of Health), CC BY-NC 2.0
- Tuniques du tube intestinal : Wikimedia Commons, by Gtaf, CC BY-SA 4.0
- Communication cellulaire : Flickr, by NIH (National Institutes of Health), CC BY-NC 2.0
- Astrocytes : Flickr, by NIH (National Institutes of Health), CC BY-NC 2.0
- Pixabay, CC0 Public Domain / Shutterstock
En cas de malaise ou de maladie, nous vous prions de consulter en tout cas un médecin ou un professionnel de la santé en mesure d’évaluer correctement votre état de santé. Le contenu de ce site https://naturolistique.fr et de ses pages annexées ne remplace en aucun cas le diagnostic d’un médecin.
https://naturolistique.fr ne permet pas de faire de diagnostic médical ou une recommandation de traitement médical pour aucune pathologie ou affection quelconque. Nous déclinons toute responsabilité en cas de mauvaise interprétation des conseils donnés.
En utilisant ce site https://naturolistique.fr , vous reconnaissez avoir pris connaissance de l’avis de désengagement de responsabilité et vous consentez à ses modalités.
![]()